
頌栄女子学院中学校過去問研究
2016年度頌栄女子学院中学校理科入試問題から、3.ものの燃焼を解説します。ガスバーナーの使用手順と金属と酸素が結びつくときの重さの計算を学習しましょう。

中学受験指導はスペースONEのプロ家庭教師にお任せください。

2016年度頌栄女子学院中学校理科入試問題から、3.ものの燃焼を解説します。ガスバーナーの使用手順と金属と酸素が結びつくときの重さの計算を学習しましょう。
| 問1 燃焼するためには酸素と熱の他に何が必要ですか。 |
| 解説解答 |
| 物が酸素と結びつき、熱や光を出す現象を燃焼といいます。物が燃えるのに必要な3つの要素を「燃焼の3要素」といいます。 燃焼の3要素は、① 燃える物があること ② 燃やすための気体(酸素)があること。③ 物の温度が発火点以上になることです。 |
| 答 燃える物があること |
| 問2 ガスバーナーの使い方について答えなさい。 (1) ガスバーナーをつけ、その炎を適切に調整する手順を、次のア~エを正しく並べ換えて、左から書きなさい。 ア ガスの元栓を開け、コックを開ける。 イ ガス調整ねじを回して開ける。 ウ 空気調節ねじを回して開ける。 エ ガスバーナーの口にマッチの炎を近づける。 |
| 解説 |
| 火を付けるときは元栓→ガス→空気の順番で、逆に消す時は、空気→ガス→元栓の順番です。 火を付けるときの手順は 1 空気調節ねじとガス調節ねじがしまっている事を確認する。 2 ガスの元栓を開く。 3 マッチに火を付けガス調節ねじを回して適当な炎の形にする。 4 空気調節ねじを少しずつ回し炎を青色にする。 5 熱する 火を消すときの手順は 1 空気調節ねじを回して炎を赤色に戻す。 2 ガス調節ねじを回して炎を消す。 3 元栓を閉じる よって 1.ア ガスの元栓を開け、コックを開ける。2.エ ガスバーナーの口にマッチの炎を近づける。3.イ ガス調整ねじを回して開ける。 4.ウ 空気調節ねじを回して開ける。 |
| 答 ア,エ,イ,ウ |
| (2) ガス調節ねじはどちらの向きに回せば開けることができますか。次のア,イから1つ選んで、記号で答えなさい。 ア 時計回り イ 反時計回り |
| 解説 |
|
ねじは上から見て反時計回りの回転 → 開く。上から見て時計回りの回転 → 閉じる。 ねじの調節は ガス → 空気の順で、ガスの炎の色は青色になるようにする。 |
| 答 イ 反時計回り |
| (3) 図1のガスバーナーのコックはどのような状態ですか。次のア,イから1つ選んで、記号で答えなさい。 ア 開いている イ 閉じている |
| 解説 |
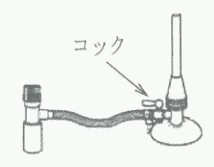 |
| ガスホースと平行になっているときは開いている。 |
| 答 ア 開いている |
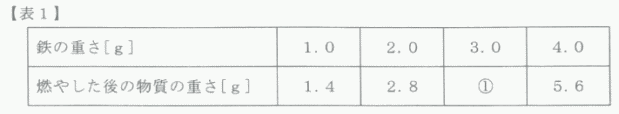
| 表1の空欄①に当てはまる数値を求めなさい。 | ||
 |
||
| 解説 | ||
| 鉄の重さが2倍・3倍・・・となると燃やした後の物質の重さも2倍・3倍・・・となる。(比例の関係) よって 比例式より 1.0:3.0 = 1.4:① ① = 1.4×3.0÷1.0 = 4.2 |
||
| 答 4.2g | ||
| マグネシウムの粉1.2gを完全にもや宇土燃やした後の物質の重さは何gになるか答えなさい。 | ||
| 解説 | ||
| マグネシウムの重さと燃やした後の物質の重さも比例するので よって 比例式より 5:3 = χ:1.2 χ = 1.2×5÷3 = 2.0 |
||
| 答 2g | ||
| 問5 鉄やマグネシウムのような金属を燃やすと重さが増えるのは、燃やすのに必要な酸素と結びついて違う物質になるためです。 (1) 表1より、鉄の粉4.0gがすべて燃えたとき、鉄に結びついた酸素の重さは何gか答えなさい。 |
|
| 解説 | |
 |
|
| 鉄の粉4.0gがすべて燃えたとき燃やした後の物質の重さは5.6g 鉄を燃やすときに、鉄が酸素と結びついた分だけ重くなるので 5.6 - 4.0 = 1.6 |
|
| 答 1.6g | |
| (2) 同じ重さの酸素に結びつく鉄とマグネシウムの重さの比を、最も簡単な整数比で求めなさい。 | |
| 解説 | |
| (1) より鉄の粉4.0gと、鉄に結びついた酸素の量は1.6g よって 鉄と酸素が結びつく割合の比は 4.0:1.6 = 5:2 | |
| マグネシウム3gが完全に燃えた後の物質の重さは5gなので、マグネシウム3gと結びついた酸素の重さは5 - 3 = 2g よって マグネシウムと酸素が結びつく割合の比は3:2 連比より 鉄:マグネシウム = 5:3 |
|
| 答 鉄:マグネシウム = 5:3 |
| 問6 鉄2.5gとマグネシウム4.2gを混ぜた粉を用意しました。この粉をすべて燃やすのに必要な酸素の重さは何gですか。 | |
| 解説 | |
| 鉄2.5gを燃やすのに必要な酸素の重さは 鉄と酸素の割合の比より 5:2 = 2.5:χ χ = 2×2.5÷5 =1g マグネシウム4.2gを燃やすのに必要な酸素の重さは マグネシウムと酸素の割合の比より 3:2 = 4.2:χ χ = 2×4.25÷3 =2.8g よって 1 + 2.8 = 3.8 |
|
| 答 3.8g |
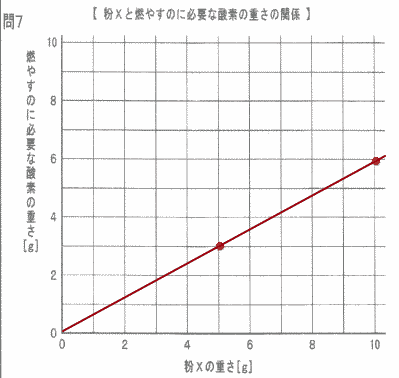
| 問7 鉄とマグネシウムを重さの比1:3で混ぜた粉Xを用意しました。この粉Xをすべて燃やすときの、粉Xの重さと燃やすのに必要な酸素の重さとの関係をグラフで表しなさい。ただし、縦軸は酸素の重さ、横軸は粉Xの重さを表します。 | |
| 解説 | |
| すべて燃やすときの鉄と酸素の割合の比は 鉄:酸素 = 5:2 すべて燃やすときの鉄とマグネシウムと酸素の割合の比は マグネシウム:酸素 = 3:2 粉Xは鉄とマグネシウムを重さの比1:3で混ぜているので、マグネシウムの重さが鉄5の3倍15のとき必要な酸素の重さは2×15÷3 = 10 よって 鉄 + マグネシウム:酸素 = 5 + 15 :2 + 10 = 20:12 = 5:3 粉Xの重さ:酸素 = 5:3 の割合でグラフをかくとよい。 |
|
| 答 | |
 |